wissen.de Artikel
Wie vor 150 Jahren das Periodensystem der Elemente entstand

Rätselhafte "Verwandtschaften"
Mitte des 19. Jahrhunderts waren die Chemiker dann schon etwas weiter: Sie hatten inzwischen zahlreiche Elemente identifiziert und auch deren Atomgewichte ermittelt. Und dabei stellten sie auffallende Ähnlichkeiten fest: So waren beispielsweise die Elemente Chlor, Brom und Iod alle drei gasförmig oder leicht flüchtig, dabei intensiv gefärbt und mit Metallen extrem reaktionsfreudig. Andere, wie Lithium, Natrium und Kalium waren dagegen fest und reagierten stark mit Wasser.
Der englische Chemiker John Reina Newlands erkannte, dass diese "Verwandtschaft" bestimmter Elemente mit ihren Atomgewichten zusammenhängt. Denn reiht man die bekannten Elemente nach größer werdender Atommasse auf, ergibt sich ein Muster: Nach jedem achten Element wiederholen sich die grundlegenden Eigenschaften. Newslands tauft seine Entdeckung daher „Gesetz der Oktaven“. Allerdings hat sein Muster auch einige Ausreißer – Elemente, die sich einfach nicht ins System fügen wollen.
Auf die Valenzen kommt es an
Eine Lösung für dieses Rätsel sucht auch Dmitri Mendelejew. Anfang 1869 verschanzt sich der Professor für reine Chemie an der Universität von Sankt Petersburg deswegen wochenlang in seinem Büro. Außer für seine Vorlesungen hat er für nichts mehr Zeit. Denn wie viele seiner Zeitgenossen ist er der Grundordnung der Elemente auf der Spur – und er ist ganz dicht dran, das spürt er. Ähnlich wie John Newlands hat auch Mendelejew längst erkannt, dass es eine Verbindung zwischen den Atomgewichten und den Eigenschaften der chemischen Elemente geben muss.
Doch im Gegensatz zu seinen Zeitgenossen berücksichtigt Mendelejew noch einen weiteren Faktor: die Valenz oder Wertigkeit. Diese Eigenschaft von Elementen gibt an, wie groß ihre Bindungsfähigkeit ist. Oder anders ausgedrückt: Wie viele „freie Ärmchen“ jedes Atom besitzt, um sich mit anderen Atomen zusammenzulagern. Mendelejew stellt fest, dass sich auch die Valenzen der Elemente periodisch zu wiederholen scheinen: Von Lithium bis Fluor steigen sie von eins bis sieben an, dann beginnt Natrium wieder bei eins und die Valenzen steigen erneut bis Chlor an.

Das erste Periodensystem
Doch wie lassen sich die Atomgewichte und Valenzen in ein gemeinsames System bringen? „In meinem Kopf kommt alles zusammen, aber ich kann es nicht ausdrücken“, schildert Mendelejew seinem Problem einem Freund. Doch er gibt nicht auf. Für seine Überlegungen hat er sich Pappkärtchen angelegt – für jedes Element eines. Auf jedem stehen die Atommasse und die prägendsten Eigenschaften einschließlich der Valenzen. Diese Elementkarten schiebt Mendelejew so lange auf seinem Tisch herum, bis alles zusammenpasst.
Plötzlich scheint alles ganz einfach: Die Elemente bilden sieben Gruppen, die jeweils senkrecht untereinander Stoffe mit ähnlichen Eigenschaften vereinen. Diese Gruppen sind wiederum so nebeneinander angeordnet, dass in den Zeilen – den Perioden – des Systems die Atommassen und Valenzen der Elemente aufsteigen. Den Anfang machen die Alkalimetalle, gefolgt von der Gruppe der Erdalkalimetalle. Dann folgen die „Erdmetalle“ angeführt von Bor, die Kohlenstoff-, die Stickstoff- und die Sauerstoffgruppe. Den Abschluss bilden die Halogene mit Fluor, Chlor, Brom und Iod.
Damit hat der russische Chemiker das Geheimnis der chemischen Elemente geknackt: Am 6. März 1869 veröffentlicht Mendelejew sein erstes Periodensystem der Elemente. Als erstem ist es ihm gelungen, nicht nur die Elemente sinnvoll zu ordnen, sondern auch die Gesetzmäßigkeiten hinter ihren Eigenschaften aufzuzeigen. Und nicht nur das: Lücken in seiner Tabelle zeigen an, wo noch Elemente fehlen – Stoffe, die bisher noch nicht entdeckt wurden.
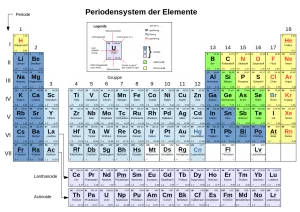
Gültig bis heute – und immer für eine Überraschung gut
Heute bildet das Periodensystem der Elemente eine wichtige Grundlage der Chemie – diese Tafel hängt nicht umsonst in den Chemieräumen jeder Schule. Denn die Position eines Atoms in dieser Tabelle spiegelt seine fundamentalen Eigenschaften wider – die Zahl seiner Kernbausteine und Elektronen, aber auch sein Bindungsverhalten, seine Stabilität und die Ähnlichkeit zu anderen Elementen.
Inzwischen umfasst das Periodensystem 118 Elemente - und es könnte noch weiter wachsen. Denn viele der ultraschweren Elemente sind so kurzlebig, dass sie erst in jüngster Zeit in den Laboren der Kernphysiker erzeugt werden konnten. Die Elemente 113, 115, 117 und 118 beispielsweise erhielten erst im Jahr 2016 ihre offiziellen Namen. Sie vervollständigen die siebte und vorerst unterste Periode in der Elemente-Tafel.
Aber auch in den altbekannten Regionen des Periodensystems verbergen sich noch immer Überraschungen. So verhalten sich die Erdalkalimetalle Calcium, Barium und Strontium in chemischen Reaktionen anders als lange angenommen – und anders, als es ihre Position im Periodensystem nahelegt. Denn statt nur acht Elektronen sind an einigen ihrer Bindungen sogar 18 Elektronen beteiligt. Das ist für Elemente der sogenannten Hauptgruppen des Periodensystems extrem ungewöhnlich.
Auch wenn das Periodensystem schon 150 Jahre auf dem Buckel hat, ist es doch bis heute der wichtigste Wegweiser der Chemie – und es hat noch immer einiges an Überraschungen parat.