Wissensbibliothek
Reduktion und Oxidation: Am Anfang stand das Feuer
Was haben das Rosten von Eisen und das Laden einer Batterie gemein?
Bei beiden Vorgängen laufen – wie auch bei vielen anderen Prozessen, etwa dem Verbrennen von Holz oder Öl – chemische Reaktionen vom gleichen Typ ab: Elektronenübertragungsreaktionen, bei denen in der Sprache der Chemiker ein Reaktionspartner oxidiert und der andere reduziert wird. Neben den Säure-Base-Reaktionen handelt es sich bei diesen Vorgängen um einen der häufigsten Reaktionstypen, der auch in Biologie und Alltag unzählige Male auszumachen ist: so beim Atmen, im Automotor oder bei der Anwendung von Sanitärreinigern.
Was ist eine Redoxreaktion?
Die Abkürzung für »Reaktion, bei der Oxidation und Reduktion zugleich ablaufen«. Das Wort »Oxidation« kommt vom wissenschaftlichen Namen des Sauerstoffs, Oxygenium (O). Früher dachte man, das Entscheidende etwa bei einer Verbrennung sei die Anlagerung von Sauerstoffatomen: Wird beispielsweise der in einem Stück Kohle enthaltene Kohlenstoff (C) verbrannt, so entsteht dabei Kohlenstoffdioxid oder kurz Kohlendioxid (CO2) – der Kohlenstoff ist »oxidiert«. Im umgekehrten Fall, etwa bei der Fotosynthese in den Blättern eines Baums, wird der Sauerstoffgehalt des aus der Luft aufgenommenen Kohlendioxids reduziert (nämlich von zwei O-Atomen pro C-Atom auf eines im Produkt Glucose), daher der Begriff »Reduktion«. Erst später wurde erkannt, dass bei diesem Reaktionstyp die Übertragung von Elektronen das eigentlich Entscheidende ist. Mittlerweile kennt man viele Redox-Reaktionen, an denen keinerlei Sauerstoff beteiligt ist, die aber dennoch nach demselben Schema wie die »klassische« Kohlenstoffverbrennung ablaufen.
Was ist das Besondere am Sauerstoff?
Von allen chemischen Elementen nehmen Sauerstoff und Fluor am bereitwilligsten Elektronen auf. Und während das extrem aggressive Fluor auf der Erde recht selten vorkommt, ist Sauerstoff eines der häufigsten Elemente unseres Planeten: Fast die Hälfte der Erdkruste besteht aus Sauerstoff. Die Tatsache, dass dieses Element so begierig auf Elektronen ist, lässt es mit praktisch jedem anderen Element Verbindungen eingehen, wobei meist große Energiemengen freigesetzt werden. Dies merkt nicht nur das »gebrannte Kind«, das seine Hand ins Feuer gehalten hat (Verbindung von Kohlenwasserstoffen mit Sauerstoff), sondern auch der Chemielehrer, dem die gefürchtete Knallgasreaktion von Wasserstoff und Sauerstoff außer Kontrolle geraten ist.
Warum heißt es eigentlich »wasserstoffblond«?
Aufgrund eines Missverständnisses bzw. einer sachlich nicht ganz richtigen Verkürzung. Verantwortlich für die Aufhellung der Haare beim Blondieren ist nämlich ein Sauerstoffatom (O). Wenn sich dieses an ein Wassermolekül (H2O) anlagert, entsteht das hochreaktive Wasserstoffperoxid (H2O2). Nach diesem Molekül ist das Verfahren offiziell benannt, doch die Umgangssprache verkürzte das etwas sperrige Wort »wasserstoffperoxidblond« zu »wasserstoffblond«. Chemisch passiert dabei Folgendes: Das Wasserstoffperoxid gibt sein überzähliges Sauerstoffatom ab. Dieses oxidiert umgehend ein Farbstoffmolekül im Haar (z. B. das dunkle Melanin) und nimmt ihm so seine Wirkung, wodurch bei genügendem Einsatz des Bleichmittels die Haare einen oft unnatürlich hell wirkenden Farbton bekommen.
Gibt es auch biologische Redoxreaktionen?
Ja, auch im Menschen (und in allen Tieren und Pflanzen) laufen unzählige Redoxreaktionen ab; eine der wichtigsten davon ist der Abbau von Glucose beim Verdauen einer zucker- oder stärkehaltigen Mahlzeit. Als zweiter Redoxpartner neben der Glucose fungieren sog. Coenzyme. Der Name »kalte Verbrennung« für diese biochemischen Abbaureaktionen rührt daher, dass wie bei einer echten Verbrennung am offenen Feuer letztlich Kohlen(wasser)stoffe reduziert werden und Kohlendioxid als Abbauprodukt entweicht. Der Unterschied ist aber, dass hier die Reaktionsenergie nicht als Hitze, sondern in chemischer Form freigesetzt wird. Dies ist nicht nur schonender für das Körpergewebe, sondern auch wesentlich effizienter, weil kaum Energie ungenutzt verloren geht.
Sind Antioxidantien gesund?
Im Prinzip ja – aber nicht alle bzw. nicht ausschließlich. Vielen Lebensmitteln (und u. a. auch Kunststoffen) werden sog. Antioxidantien zugesetzt, die deren Oxidation verhindern sollen. Andernfalls können beispielsweise angebissene bzw. aufgeschnittene Äpfel braun, andere Speisen sogar ungenießbar werden. In Obst und Gemüse, angeblich auch in Kaffee enthaltene Antioxidantien sollen darüber hinaus auch die Gesundheit der Konsumenten fördern, indem sie die Oxidation von wichtigen körpereigenen Molekülen hemmen. Diese gilt derzeit als Ursache oder wichtige Begleiterscheinung verschiedener Alterungsprozesse. Manche Antioxidantien gelten aber als Krebs fördernd oder anderweitig schädlich, so dass eine unüberlegte Überdosierung nicht zu empfehlen ist.
Wussten Sie, dass …
viele Reinigungsmittel Oxidations- oder Reduktionsmittel enthalten?
beim versehentlichen Zusammenmischen von chloridhaltigen und hypochlorithaltigen Sanitärreinigern giftiges Chlorgas entstehen kann? Auch dies ist eine Redoxreaktion.
Die Vitamine C und E natürliche Antioxidantien sind? Dies zeigt ein alter Trick aus dem Haushalt: Wenn man auf einen frisch aufgeschnittenen Apfel Zitronensaft träufelt, wird das unschöne Braunwerden der Schnittfläche verhindert.
»Rost« eine Sammelbezeichnung für verschiedene Eisenoxide ist, die sich bilden, wenn Eisen in feuchter Umgebung mit Luftsauerstoff reagiert?

Wanderkarte der Huftiere hilft Gazelle und Co zu schützen
Ob Rentier, Gämse oder Gnu: Huftiere legen regelmäßig große Distanzen zurück und treffen dabei immer häufiger auf menschengemachte Hürden wie Schienen. Wissenschaftler haben nun erstmals die weltweiten Wanderbewegungen von 20 Huftierarten in einer digitalen Karte zusammengefasst. In dem Online-Atlas sind die detaillierten Routen...
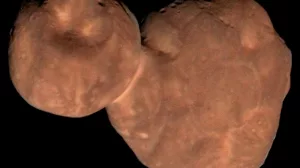
Portrait eines Außenseiters
Jenseits von Pluto gibt es urtümliche Fels- und Eisbrocken wie sonst nirgendwo im Sonnensystem. Die Raumsonde New Horizons hat erstmals einen davon aus der Nähe inspiziert. von THORSTEN DAMBECK Am Neujahrstag 2019 passierte die Raumsonde New Horizons in 3538 Kilometer Minimalabstand ein seltsames Objekt namens Arrokoth. In einer...

